Ministerio de Salud Pública RDDirección General EpidemiologíaBoletín•45•Coronavirus(COVID-19)SituaciónRD, 2/5/2020 18:00•Casos confirmados:7,954•Casos nuevos:376•Fallecidos:333•Tasa letalidad:4.19%•Recuperados:1606•Descartados:24,071•Muestras procesadas:32,025
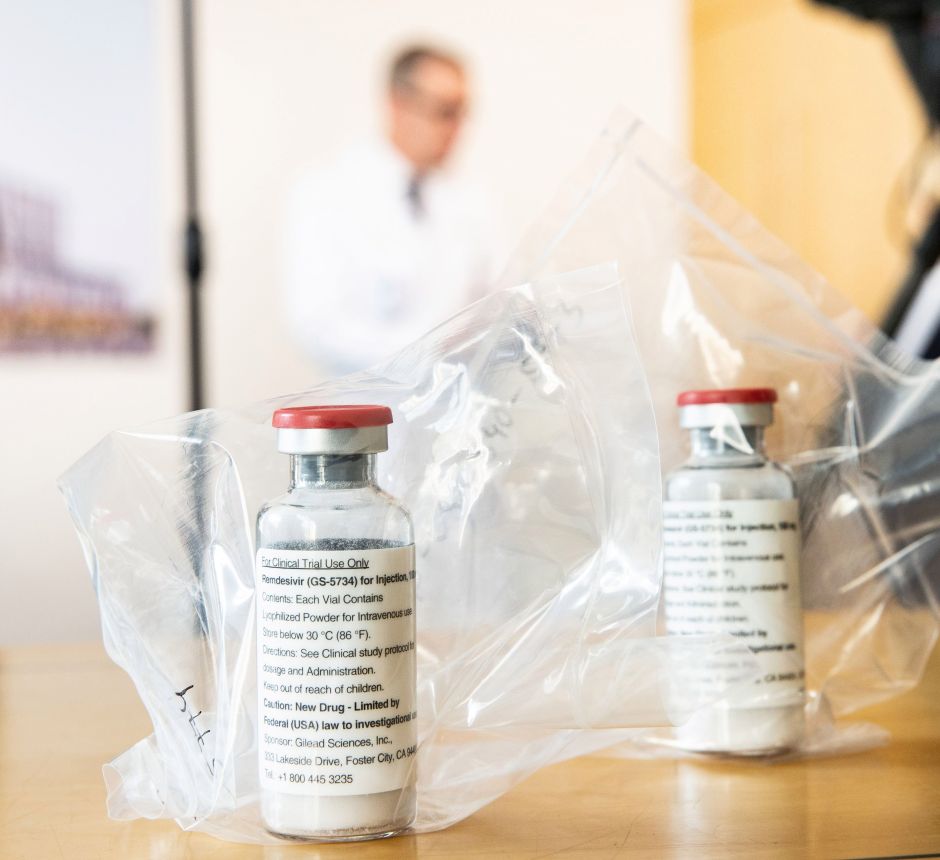
FDA aprueba el fármaco Remdesivir para uso de emergencia en pacientes con COVID-19
La aprobación de emergencia permite que el medicamento llegue al mercado
Por:
Remdesivir, el fármaco antiviral de la compañía Gilead Sciences, ha sido aprobado por la Administración de Drogas y Alimentos de Estados Unidos (FDA) para uso de emergencia en pacientes con COVID-19, informó este viernes el presidente Donald Trump desde la Casa Blanca.
La autorización se da en el momento que el medicamento mostró resultados positivos al ayudar a los pacientes hospitalizados a recuperarse de una manera más rápida.
La aprobación del fármaco por parte de la FDA se hizo mediante el uso de emergencia, un paso por el cual la agencia puede llevar los productos al mercado sin datos completos sobre su seguridad y eficacia, por lo que la agencia continuará realizando más estudios sobre el medicamento.
Durante la reunión en el Despacho Oval, Daniel O’Day, director ejecutivo de Gilead Sciences Inc, calificó la medida como un primer paso importante y dijo que “para asegurarnos de que nada se interponga en el camino de estos pacientes para obtener el medicamento” la empresa donará 1.5 millones de ampolletas del fármaco, reportó la agencia Reuters.
Hasta ahora los medicamentos que habían recibido la autorización de emergencia contra el COVID-19 eran la hidroxicloroquina y cloroquina que fueron desarrollados para tratar la malaria en pacientes hospitalizados.
Esta semana la compañía que desarrolló el fármaco informó que aplicó el tratamiento de cinco días a personas con neumonía causada por el COVID-19 produciendo mejoras en un 65% de los pacientes que permitió dar de alta a un 60% de ellos en un plazo de 14 días, mientras que solo un 8% del grupo de prueba falleció.
Relacionado: Lysol y Dettol advierten: “Bajo ninguna circunstancia se inyecte o beba nuestros productos de limpieza”
El Ramdesivir fue desarrollado para tratar otros casos de coronavirus como el SARS y fue probado ante la enfermedad provocada por el virus del Ébola.
Anthony Fauci, director del Instituto Nacional de Alergia y Enfermedades Infecciosas, dijo este jueves que los primeros resultados del fármaco tuvieron un efecto significativo en el tratamiento del COVID-19 al reducirse el tiempo de recuperación de los pacientes.
Ministerio de Salud Pública RD
Dirección General Epidemiología
Boletín•41•
Coronavirus(COVID-19)
SituaciónRD,28/4/2020 18:00
•Casos confirmados:6,652
•Casos nuevos:236
•Fallecidos:293
•Tasa letalidad:4.40%
•Recuperados:1228
•Descartados:18,716
•Muestras procesadas:25,368
Medicamento experimental contra el cáncer podría detener la infección por coronavirus
Científicos de la Universidad de Louisville han realizado ya algunas pruebas
FOTO: UNSPLASH
Una de las características de la infección por COVID-19 es la alta capacidad que tienen las células del virus para replicarse dentro del cuerpo, infectar rápidamente células sanas y producir una inflamación generalizada que, en algunos casos, puede resultar fatal.
Considerando esta particularidad, los científicos de la Universidad de Louisville, en Kentucky, están probando un medicamento experimental contra el cáncer que podría detener la infección por coronavirus. El equipo señala que el fármaco podría evitar que el virus se replique y se propague por todo el cuerpo.
De acuerdo con un comunicado de esa institución, el medicamento es una pieza de ADN sintético llamada “aptámero”. Se une a una proteína de las células llamada nucleolina, que varios tipos de cáncer y el mismo coronavirus, “secuestran” para replicarse.
El fármaco, descubierto por los doctores Paula Bates, John Trent y Don Miller, ha sido probado de diversas maneras, pero “especialmente como un posible fármaco terapéutico contra múltiples tipos de cáncer”, en asociación con el investigador Kenneth Palmer, director del Centro de Medicina Predictiva para Biodefensa y Enfermedades Infecciosas Emergentes (CPM, por sus siglas en inglés).
Ante la emergencia de salud mundial, este equipo de la Universidad de Louisville decidió probar el aptámero en células del coronavirus con buenos resultados. Sin embargo, se encuentra a la espera de la aprobación de la Administración de Alimentos y Medicamentos (FDA) para comenzar los tratamientos en pacientes graves de COVID-19.
El CPM alberga el Laboratorio de Biocontención Regional de la Universidad de Louisville, el único en Kentucky, que realiza investigaciones con agentes infecciosos en instalaciones de Nivel 3 de Bioseguridad. Según el comunicado, estas instalaciones son “estrictamente seguras y protegen a los investigadores y al público de la exposición a los patógenos que se investigan”.
Ministerio de Salud Pública RD
Dirección General Epidemiología
Boletín•36•
Coronavirus(COVID-19)
Situación RD,23/4/2020 18:00
•Casos confirmados:5,749
•Casos nuevos:206
•Fallecidos:267
•Tasa letalidad:4.64%
•Recuperados:763
•Descartados:14,521
•Muestras procesadas:20,270





No hay comentarios.:
Publicar un comentario